Серозная жидкость при операции грыжи

Послеоперационная серома – это скопление серозной жидкости в зоне шва, обусловленное травматизацией мягких тканей. Является осложнением хирургических вмешательств. Рассасывается самостоятельно либо принимает хроническое течение. Проявляется припухл остью в области шва, чувством распирания, неприятными ощущениями и эффектом переливания жидкости при перемене положения тела. При крупных серомах наблюдаются нарушение общего состояния, субфебрилитет. Патология может осложняться инфицированием, формированием некроза. Лечение – пункции или дренирование с активной аспирацией на фоне медикаментозной терапии. В отдельных случаях требуются повторные операции.
Общие сведения
Послеоперационная серома (серома шва) – распространенное осложнение раннего послеоперационного периода. Чаще всего встречается в общей хирургии, маммологии, онкологии и пластической хирургии. По различным данным, частота образования клинически значимых сером после операций, сопровождающихся значительной отслойкой мягких тканей, колеблется от 0,8% до 80% и более. Осложнение может развиваться у пациентов любого возраста и пола, чаще встречается у женщин средней и старшей возрастной группы.
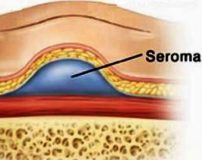
Послеоперационная серома
Причины
Серома является полиэтиологическим состоянием, рассматривается как осложнение обширных хирургических вмешательств. Некоторые специалисты придерживаются мнения, что скопление жидкости в проекции послеоперационной раны нельзя считать осложнением, поскольку оно представляет собой нормальный процесс заживления в фазе экссудации.
В подтверждение своей точки зрения ученые приводят данные ультразвуковых исследований, согласно которым послеоперационные серомы (в том числе – клинически незначимые) обнаруживаются у 100% пациентов. Основными провоцирующими факторами образования крупных сером, требующих проведения активных лечебных мероприятий, являются:
- значительная отслойка жировой клетчатки;
- большая раневая поверхность;
- грубые хирургические манипуляции с тканями (многочисленные разрезы, захват раздавливающим инструментом и пр.);
- чрезмерное использование коагуляции;
- большая толщина подкожной жировой клетчатки (более 5 см).
К числу предрасполагающих условий относят индивидуальные особенности организма, нарушения иммунитета, сахарный диабет и хронические соматические заболевания, негативно влияющие на процесс заживления раны. Чаще всего послеоперационные серомы образуются после абдоминопластики, герниопластики, маммопластики, мастэктомии, аппендэктомии, холецистэктомии. При использовании имплантатов имеет значение раздражение окружающих тканей и развитие асептического воспаления вследствие контакта с эндопротезом.
Патогенез
Существуют различные точки зрения на патогенез сером. Согласно наиболее популярной, обширные разрезы, отслойка мягкотканных структур, раздавливание или прижигание тканей и другие факторы вызывают значительные повреждения мелких лимфатических сосудов. Лимфатические сосуды тромбируются медленнее кровеносных, в результате лимфа долгое время изливается в ткани. На этапе экссудации жидкая часть крови выходит за пределы кровеносных сосудов, что увеличивает количество жидкости в тканях.
В полостях, возникших в области послеоперационной раны, скапливается соломенно-желтая жидкость, содержащая макрофаги, тучные клетки, лейкоциты и белковые фракции. В норме эта жидкость асептическая. При попадании микроорганизмов возможно нагноение с формированием абсцесса. Крупные скопления жидкости оказывают давление на окружающие ткани, нарушают кровоснабжение, вследствие чего могут образовываться участки некроза по краю швов.
Классификация
В клинической практике используют классификацию, в основе которой лежит необходимость и тактика лечения патологии. Согласно этой систематизации выделяют три группы послеоперационных сером:
- 1 группа. Асимптоматические образования, не требующие проведения лечебных мероприятий.
- 2 группа. Симптоматические серомы, для устранения которых достаточно пункций или активного дренирования.
- 3 группа. Симптоматические скопления жидкости, требующие проведения повторной операции.

Серома шва
Симптомы послеоперационной серомы
Маленькие образования не вызывают неприятных ощущений и нарушений общего состояния. Единственными признаками серомы являются припухлость и положительный симптом флюктуации в области послеоперационных швов. Иногда пациенты отмечают ощущение переливания жидкости во время изменения положения тела. Гиперемия кожи в зоне швов обычно отсутствует.
Больные с крупными серомами жалуются на неинтенсивную тянущую боль, чувство давления или распирания, которые усиливаются в положении стоя. В проекции швов выявляется валикообразная флюктуирующая припухлость. Длина припухлости обычно совпадает с длиной шва, ширина может варьироваться от 2-3 до 10 и более сантиметров. Возможны локальная гиперемия, слабость, утомляемость, повышение температуры тела до субфебрильных цифр.
Осложнения
Наиболее серьезным осложнением является нагноение серомы. При большом количестве жидкости формируются крупные абсцессы. Возможно расплавление подлежащих тканей с развитием перитонита. У некоторых больных развивается сепсис. Некрозы при серомах, как правило, протекают более благоприятно, захватывают небольшие участки тканей в области швов. Хронические серомы ухудшают качество жизни, существенно увеличивают период нетрудоспособности после операций.
Диагностика
Обычно серомы развиваются в период стационарного послеоперационного лечения, поэтому диагноз выставляется лечащим врачом. Диагностика базируется на данных объективного осмотра, при необходимости назначаются дополнительные исследования. Программа обследования может включать:
- Физикальный осмотр. В пользу серомы свидетельствует наличие ограниченного выбухания тканей в сочетании с положительным симптомом флюктуации. При отсутствии инфицирования гиперемия не выявляется или незначительная, пальпация малоболезненна. При инфицировании кожа багрово-синюшная, ощупывание резко болезненно, определяется плотный отек окружающих тканей.
- УЗИ мягких тканей. Показано для подтверждения диагноза при сомнительном симптоме флюктуации, для уточнения размеров крупных сером на этапе подготовки к хирургическому вмешательству. Свидетельствует о наличии полости, заполненной жидкостью.
- Лабораторные анализы. Для изучения характера содержимого серомы проводят цитологическое исследование. При подозрении на инфицирование выполняют бакпосев жидкости для определения возбудителя, назначают общий анализ крови для оценки выраженности воспаления.

Тактика лечения зависит от размеров серомы, наличия признаков инфицирования
Лечение послеоперационной серомы
Лечение осуществляется в стационарных условиях. При крупных образованиях, отсутствии признаков рассасывания показана комплексная терапия, включающая в себя консервативные и оперативные мероприятия.
Консервативная терапия
Целью консервативного лечения является снижение вероятности инфицирования, устранение асептического воспаления, уменьшение количества жидкости. Применяются медикаменты следующих групп.
- Антибиотики. При отсутствии нагноения пациентам для профилактики назначают препараты широкого спектра действия внутримышечно. При появлении признаков инфицирования план антибиотикотерапии корректируют с учетом чувствительности возбудителя.
- НВПС. Нестероидные противовоспалительные средства уменьшают проявления воспаления и количество жидкости, выделяющейся в просвет полости послеоперационной серомы. Возможно внутримышечное введение или пероральный прием.
- Глюкокортикоиды. Гормональные препараты устраняют асептическое воспаление, блокируют образование жидкости. Медикаменты вводят в полость серомы после удаления жидкости.
Хирургическое лечение
Тактика хирургического лечения определяется размерами серомы, эффективностью лечебных мероприятий на предыдущих стадиях. При неосложненных серомах возможны следующие варианты:
- Пункции. Наиболее простой способ удаления жидкости. Выполняется 1 раз в несколько дней, для полного излечения обычно требуется 3-7 пункций.
- Активная аспирация. При неэффективности пункций, значительном объеме серомы в полость образования устанавливают дренаж с устройством для активной аспирации.
- Реконструктивные операции. Показаны при упорном хроническом течении сером, отсутствии результата после лечения более щадящими способами.
При нагноившихся серомах производится вскрытие, дренирование гнойной полости. При образовании участков некроза проводят перевязки до отторжения струпа и полного заживления раны. Все хирургические методы применяют на фоне консервативной терапии.
Прогноз
Прогноз в большинстве случаев благоприятный. Небольшие серомы нередко рассасываются самостоятельно в течение 1-2 недель. Эффективность пункций при серомах на фоне плановых пластических и абдоминальных операций составляет около 90%. Реконструктивные вмешательства требуются редко. Процент нагноений незначительный, осложнение чаще развивается после экстренных операций, при наличии сопутствующей патологии, излишнем весе.
Профилактика
Профилактические мероприятия включают тщательную оценку риска хирургических вмешательств, детальное предоперационное обследование, соблюдение техники проведения операций. Хирургам необходимо воздерживаться от слишком широких разрезов, грубых манипуляций с тканями, чрезмерного использования коагулятора.
Источник
Раневые осложнения в области хирургического вмешательства по поводу большой послеоперационной грыжи передней брюшной стенки по-прежнему занимают лидирующие позиции среди всего спектра осложнений у этой категории пациентов [1]. Серома, или лимфоцеле, длительная серозная экссудация являются самыми распространенными осложнениями после герниопластики [2]. Их частота варьирует в широких пределах — от 0,8 до 60% [3—8].
Серому определяют как любое подкожное жидкостное скопление, выявляемое клинически и/или при УЗИ послеоперационной раны [9]. Наличие идентифицированной серомы всегда увеличивает риски некроза подкожного жирового лоскута, вторичного инфицирования, снижает репаративную возможность тканей [3, 10, 11], что в свою очередь ведет к увеличению срока пребывания пациента в стационаре, повышает экономическую нагрузку на медицинское учреждение [8], а также приводит к значительному увеличению сроков реабилитации оперированного больного [12—15].
В литературе можно встретить такие понятия, как «клиническая серома» — видимая выпуклость или флюктуация без признаков инфекции, и «субклиническая серома», выявляемая при УЗИ послеоперационной раны без отклонений при физикальном исследовании [9], а также деление сером на 3 типа:
1-й тип — асимптомные (не требуют дополнительного лечения);
2-й тип — симптомные, требующие простой пункции и аспирации;
3-й тип — симптомные, требуют повторной операции.
Частота выявления серомы может изменяться в зависимости от метода, которым ее диагностируют. По клиническим данным, эта частота будет невысока, а при УЗИ может достигать 100%. Небольшое количество жидкости в области эндопротеза выявляется практически у всех пациентов на 5—7-й день после операции. Однако жидкость обнаруживается не только в пространствах, которые непосредственно контактируют с сеткой, но и в подкожной жировой или предбрюшинной клетчатке, например при расположении эндопротеза в позиции sublay [12, 16].
Для диагностики серомы наиболее информативным методом в настоящее время является повторное УЗИ послеоперационной раны, при котором определяют скопление жидкости в подкожной клетчатке, перипротезном пространстве. УЗИ дает возможность определить скопление жидкости значительно лучше по сравнению с осмотром, особенно у пациентов с ожирением. Помимо диагностики серомы, возможно выполнение пункции и эвакуации жидкости под УЗ-контролем [17]. Метод позволяет обнаружить скопления жидкости в разных слоях послеоперационной раны, оценить эхоструктуру и эхогенность тканей передней брюшной стенки в зоне операции, дифференцировать анатомические слои. При повторных исследованиях можно оценить изменение объема жидкости и ее характер. УЗИ предоставляет информацию о положении дренажей и адекватности их функции. С помощью данных УЗИ может быть принято решение о сроках удаления дренажей [17, 18]. Этот метод признается ведущим в выявлении на ранних стадиях формирования таких осложнений, как инфильтрат, абсцесс, серома, а также может выполняться непосредственно у постели больного [19].
С.Г. Измайлов [20] выполнял УЗИ раны на 3, 5, 7, 10, 12-й день после операции. Выявлено, что при неосложненном течении послеоперационного периода ширина гипоэхогенной зоны в области мышечно-апоневротического слоя передней брюшной стенки максимально увеличивается на 3—5-й день. Ее уменьшение происходит в фазе регенерации на 7—10-й день, тогда же появляются участки с повышенной эхогенной структурой. Увеличение ширины гипоэхогенной зоны через 5—7 дней после операции без тенденции к уменьшению свидетельствует о высокой вероятности развития нагноения раны.
Четких критериев ведения пациентов с послеоперационной серомой брюшной стенки на сегодняшний день не разработано. Одни авторы активно пропагандируют пункционный способ лечения [21], другие — длительную вакуум-аспирацию [22]. Пункционное лечение под ультразвуковым контролем рекомендуют большинство авторов, которые отмечают высокую чувствительность и специфичность метода [23, 24].
Ф.Н. Ильченко и соавт. [25] отмечают значимость динамического УЗ-контроля раны и пункционного лечения сером в раннем послеоперационном периоде (в пределах 10 сут). По мнению авторов, это позволяет на ранних этапах выявить различные осложнения со стороны послеоперационной раны и вовремя профилактировать развитие нагноения. Клинически значимыми авторы считали жидкостные образования в подкожной клетчатке диаметром 3 см и более, лечение которых проводили пункционным способом под УЗ-контролем. Пункции были проведены в 25% наблюдений (всего 56 пациентов), число пункций варьировало от 2 до 8—10. Авторы сделали вывод, что использование разработанной тактики контроля состояния и ведения раны явилось эффективным способом профилактики нагноения послеоперационной раны у 97,1% пациентов.
УЗ-мониторинг состояния послеоперационной раны также нашел отражение в работе других авторов [26]. В частности, был разработан алгоритм УЗ-мониторинга послеоперационной раны после пластики послеоперационного грыжевого дефекта. Клинически значимыми скоплениями жидкости авторы считали 20 мл и более по данным УЗИ на 4—6-е сутки после операции, что требовало пункционного лечения. При получении серозно-геморрагического экссудата в объеме менее 10 мл требовалась повторная пункция через 2 сут. При схожем результате пункции прекращали. Если получали 50 мл и более, пункции повторяли ежедневно до уменьшения объема пунктата до 20 мл с контрольным УЗ-сканированием на 21-е сутки после операции. При получении жидкости во время пункции менее 50 мл повторные вмешательства проводили через 2—3 сут на протяжении 3 нед с контрольным УЗИ также на 21-е сутки и при положительной динамике (менее 20 мл) на 28-е сутки. Если по данным УЗИ на 4—6-е сутки после операции выявлялось жидкостное образование менее 20 мл, проводили контрольное УЗИ перед снятием швов (на 10—13-е сутки). Авторами работы был сделан вывод, что с 95% вероятностью предложенный алгоритм УЗ-мониторинга послеоперационной раны позволяет снизить общую частоту раневых осложнений. Однако такой алгоритм не лишен и недостатков, так как ежедневное повторение пункций на основании только однократного выявления жидкостного скопления в послеоперационной ране в объеме 50 мл грозит увеличением инфекционных осложнений, а также причиняет физическое и психологическое страдание пациенту.
А.Г. Измайлов и соавт. [27] в послеоперационном периоде всем пациентам на 3, 5 и 7-е сутки проводили УЗИ с целью контроля течения раневого процесса и при увеличении объема образований послеоперационных ран более 4 см3, проводили под УЗ-контролем пункцию с помощью аспирационной иглы.
В работе Н.К. Тарасовой и соавт. [28] описано выполнение пункции серомы под УЗ-контролем при скоплении жидкости более 20 мм. Закрытый способ ведения раны позволил авторам избежать высокой частоты гнойных осложнений, которая составила 0,32%.
А.В. Кузнецов и соавт. [29] провели работу, в которой были проспективно изучены результаты лечения 183 пациентов, оперированных по поводу послеоперационной вентральной грыжи с установкой сетчатого импланта onlay, послеоперационный период которых сопровождался формированием серомы. Пациенты были разделены на четыре группы в зависимости от способа опорожнения жидкостных образований: а) опорожнение через рану перчаточным выпускником; б) опорожнение через рану без дренажа с ежедневным зондированием линии швов; в) опорожнение полости серомы, установка вакуум-дренажа в полость серомы на 3 сут через отдельный прокол, минуя линию швов; г) пункционный способ. После 12 сут при сохранении экссудации всех больных из любой группы переводили на пункционное опорожнение серомы на 21, 36 и 45-е сутки. Лидерами по количеству экссудата явились группы с постоянным нахождением инородного тела (дренажной трубки) в ране. Авторы связывают это с раздражающим действием дополнительного инородного тела в брюшной стенке и активного движения интерстициальной и внутрисосудистой жидкости под действием вакуума. При количестве экссудата менее 5 мл пункции полностью прекращали. Минимально осложнения присутствовали в группе с пункционным ведением послеоперационного периода. Авторы пришли к следующим выводам: наименее желательным способом ведения сером является опорожнение полости с оставлением дренажной резиновой полоски; использование в раннем послеоперационном периоде вакуумного дренажа по Редону при грыжах среднего размера не имеет преимуществ перед пункционным методом; оптимальным для лечения сером после аллопластики грыжевого дефекта является пункционный способ. Это подтверждается на 11,1—27,2% более скорым исчезновением экстравазата, на 9,7—39,4% меньшим риском инфицирования полости серомы, более благоприятным и на 25,6—39,6% более краткосрочным восстановительным периодом.
Таким образом, лечение пациентов с большой послеоперационной вентральной грыжей, у которых течение послеоперационного периода осложнилось образованием серомы, является актуальной и не до конца изученной проблемой. Стандартом диагностики признано повторное УЗИ состояния послеоперационной раны, а лечения — пункционная аспирация серомы.
В настоящее время не разработано четкого и простого алгоритма диагностического мониторинга и лечения при острых жидкостных скоплениях у пациентов после пластики большого послеоперационного грыжевого дефекта передней брюшной стенки с использованием сетчатого эндопротеза, дифференцированного подхода к этой проблеме. Разработка гибкого подхода к данной проблеме с использованием УЗ-мониторинга по сей день актуальная и важная тема.
Авторы заявляют об отсутствии конфликта интересов.
Источник
